A la une
Si aucune action n’est prise, des millions de décès pourraient, chaque année, être imputés à des maladies causées par des bactéries résistantes aux antibiotiques d’ici 2050. Pour y remédier, des chercheurs ambitionnent de décrypter certains mécanismes de résistance encore énigmatiques, tandis que d’autres préparent le terrain pour de nouvelles stratégies de ciblage de ces médicaments.
Plus silencieuse mais également plus ancienne que la Covid-19, l’antibiorésistance n’en est pas moins une menace majeure pour la santé mondiale. L’efficacité de nombreux traitements antibiotiques est en effet compromise en raison de la capacité croissante des bactéries pathogènes à échapper à ces stratégies thérapeutiques.
Christophe Grangeasse, directeur de Recherche CNRS au laboratoire microbiologie moléculaire et biochimie structurale1, exprime son inquiétude en rappelant qu’en 2014, une étude britannique alertait déjà sur l’importance « de découvrir de nouvelles molécules capables d’échapper aux processus d’antibiorésistance, sans quoi le nombre de décès liés aux bactéries pourrait atteindre 10 millions de personnes et dépasserait celui des décès dus aux cancers d’ici 2050 ».
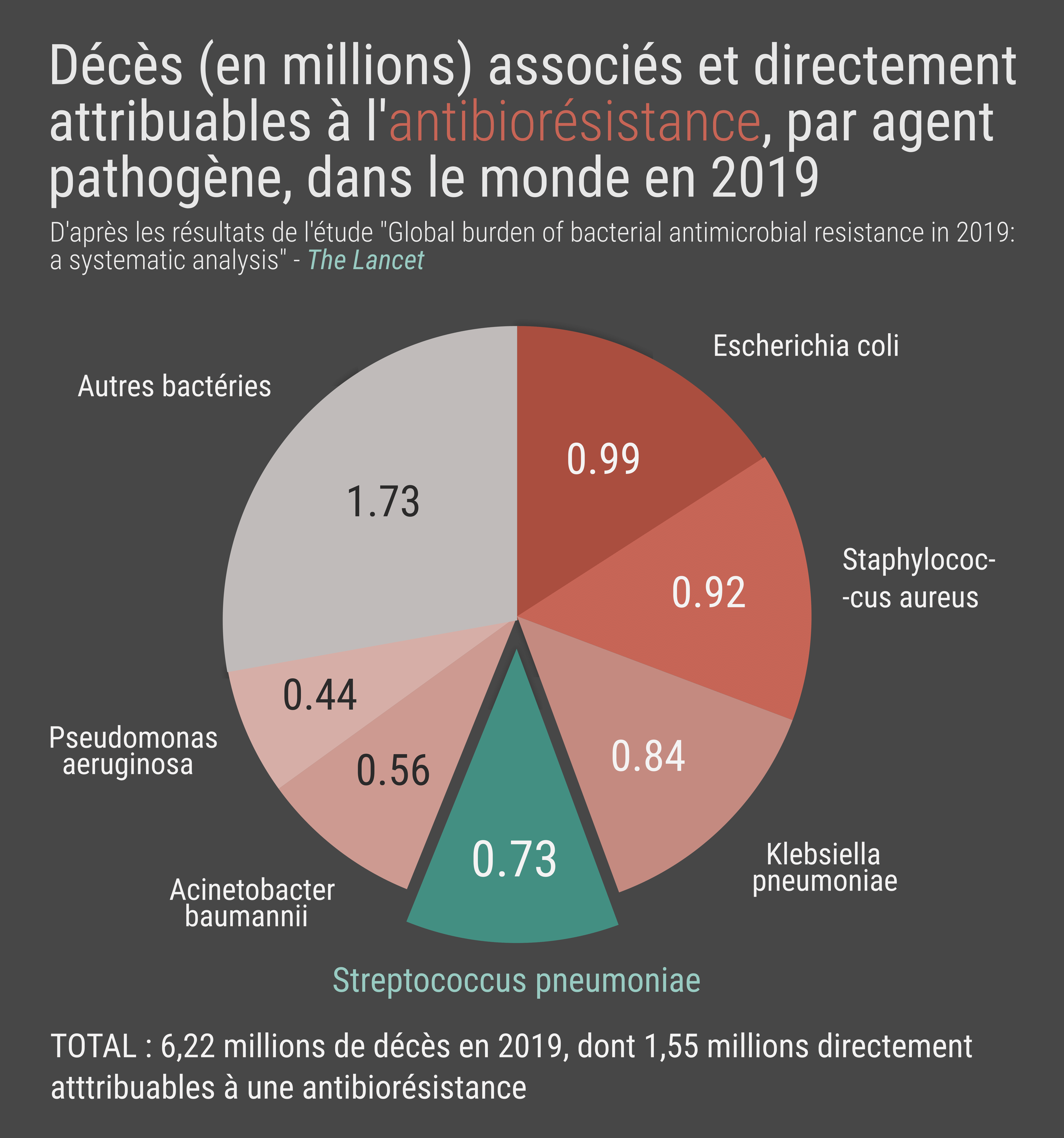 Décès associés et directement attribuables à l'antibioresistance, par agent pathogène, dans le monde en 2019 © Samuel Belaud
Décès associés et directement attribuables à l'antibioresistance, par agent pathogène, dans le monde en 2019 © Samuel Belaud
Le phénomène est d’autant plus alarmant que « contrairement aux cancers qui touchent majoritairement les personnes plus âgées, les infections bactériennes – elles – s’attaquent à l’ensemble de la population et notamment aux enfants » souligne le récent médaillé d’argent du CNRS.
Une pandémie silencieuse
Cédric Orelle, directeur de Recherche CNRS dans la même unité, tient à rappeler que « les antibiotiques ont, avant toute chose, révolutionné la médecine moderne. Avant les années 1940, la moindre infection pouvait nous être fatale ! » Néanmoins, il relève aussi que depuis, leur utilisation inappropriée et abusive « y compris dans le contexte des élevages industriels a généré de graves problèmes ».
Des générations de bétail ont en effet été exposées à ces molécules, rendant certaines bactéries de plus en plus résistantes et contraignant les éleveurs à recourir à des doses d’antibiotiques encore plus élevées. En outre, près de la moitié des antibiotiques fabriqués à travers le monde sont destinés à l’élevage et ce chiffre grimpe à 80% aux États-Unis. Une surutilisation qui a entraîné la présence de traces résiduelles d’antibiotiques dans l’environnement : des eaux usées, jusque dans nos assiettes.
La recherche en ordre de bataille
« Par ailleurs, commente Cédric Orelle, les rejets de nombreuses autres molécules dans l’environnement (antiseptiques, pesticides, polluants, etc.) ont aussi pu contribuer à la sélection de bactéries résistantes à ces molécules ainsi qu’à certains antibiotiques ». Combinée avec une administration excessive chez l’humain, cette situation a favorisé la prolifération de bactéries résistantes et l’inefficacité d’un nombre croissant de traitements contre certaines infections.
Face à cette menace grandissante, « la recherche scientifique mondiale peine à trouver des molécules avec de nouveaux modes d’action » souligne Christophe Grangeasse. Les avancées les plus récentes en matière de traitements d’infection bactérienne consistent essentiellement en des modifications d’antibiotiques déjà existants. Dès lors, sous l’impulsion de l’Organisation Mondiale de la Santé (OMS) et des agences nationales de recherche, les scientifiques du monde entier se sont récemment remis en ordre de bataille pour trouver de nouvelles stratégies de lutte et prévenir une crise sanitaire mondiale. Un combat qui débute par une étape fondamentale : infiltrer les rangs de l’adversaire pour acquérir une connaissance approfondie de ses mécanismes de fonctionnement.
Infiltrer les rangs ennemis
On sait d’ores et déjà que les cellules bactériennes disposent de plusieurs moyens de défense qu’elles peuvent combiner avec une efficacité redoutable. Cédric Orelle les énumère : « elles peuvent acquérir des mutations sur les gènes codant la cible de l’antibiotique ; freiner l’entrée de l’antibiotique dans la bactérie ; exprimer une protéine qui inactive l’antibiotique ; ou enfin, mon sujet d’étude, utiliser certaines protéines membranaires pour rejeter les antibiotiques hors de la bactérie ».
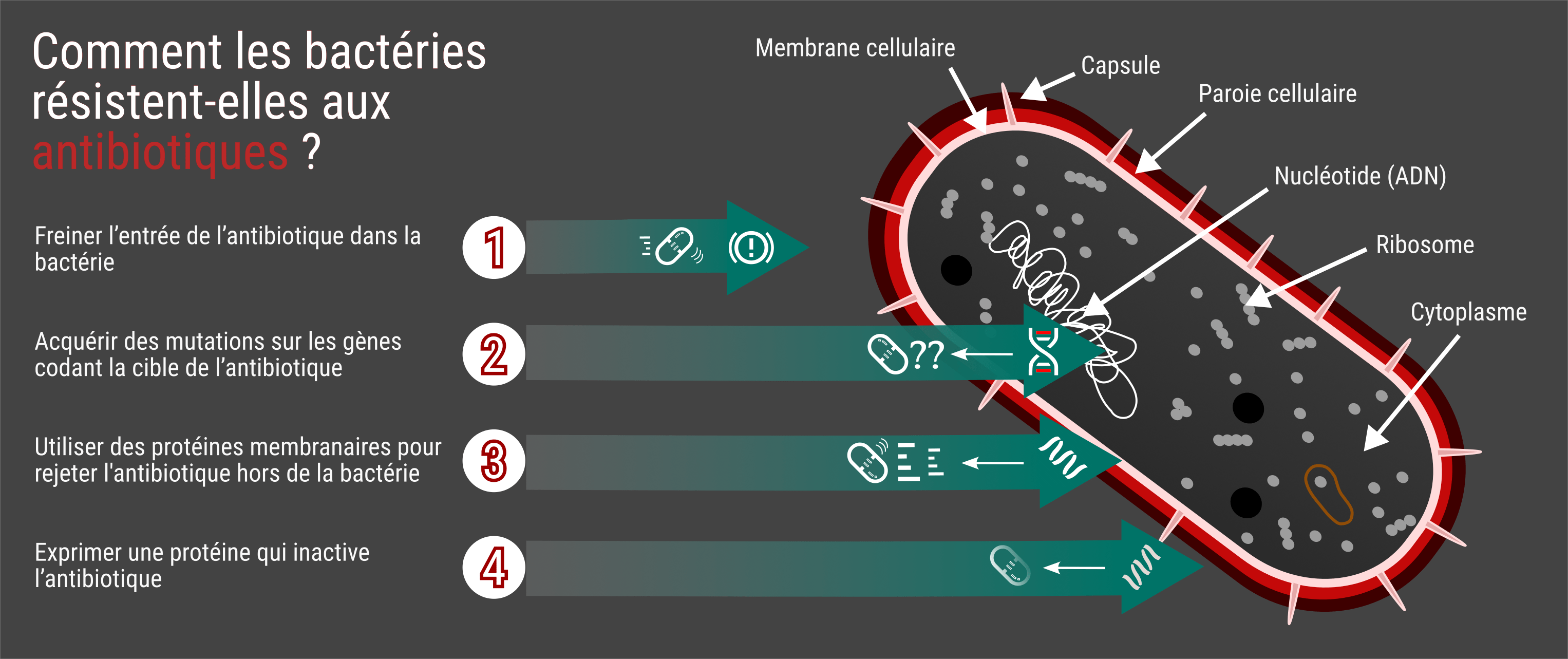 Mécanismes de résistance des bactéries. © Samuel Belaud
Mécanismes de résistance des bactéries. © Samuel Belaud
C’est par une analyse approfondie de tous ces facteurs de résistance que les scientifiques espèrent faire émerger de nouvelles solutions pour les contourner. Une des stratégies consiste à explorer de nouvelles voies de régulation des bactéries. Autrement dit, il s’agit de décrypter les mécanismes qui permettent aux cellules bactériennes de contrôler et d’ajuster leur réponse à différents signaux extérieurs.
Découvrir de nouvelles cibles
« C’est une approche novatrice, souligne Christophe Grangeasse, qui se souvient qu’au début des années 2000, un dogme scientifique prédominant soutenait que les bactéries – contrairement aux cellules eucaryotes2 – étaient dépourvues d’un ensemble de protéines régulatrices que l’on appelle des sérine/thréonine protéines kinases (PK) ». Il est maintenant clairement établi que ces PK jouent un rôle central dans la capacité des bactéries à se multiplier et à s’adapter à leur environnement. « Il s’agit d’une avancée fondamentale, insiste le chercheur, car ces protéines pourraient, à terme, être considérées comme de nouvelles cibles thérapeutiques ».
« En utilisant une approche interdisciplinaire alliant l’imagerie cellulaire, la génétique et la biochimie structurale, poursuit-il, nous nous sommes rendu compte que ces PK exerçaient une influence considérable sur l’intégrité de la cellule bactérienne, et donc sur leur survie ». Les travaux que mènent Christophe Grangeasse et son équipe visent donc à décrypter ces mécanismes de régulation pour, à terme, imaginer des traitements qui puissent directement cibler les PK. Ce nouveau type de médicament affecterait la viabilité de la bactérie et l’empêcherait de s’adapter à son environnement et donc de provoquer une infection.
Les pneumocoques, modèles de résistance
Parmi les bactéries particulièrement concernées par la résistance aux antibiotiques qu’étudie le chercheur, le pneumocoque tient une place de choix. Chaque année, malgré l’existence d’un vaccin et d’antibiotiques efficaces, plus d’1,5 million de personnes meurent des suites des conséquences d’une infection par la bactérie Streptococcus pneumoniae dans le monde. Ce pouvoir infectieux s’explique notamment par un des modes de survie du pneumocoque, qui consiste à “assimiler” de l’ADN exogène (qui peut provenir d’autres organismes) et de manipuler ensuite son propre génome de façon à pouvoir acquérir rapidement des mutations. Celles-ci lui permettent ensuite de résister aux traitements antibiotiques et même d’échapper aux vaccins.
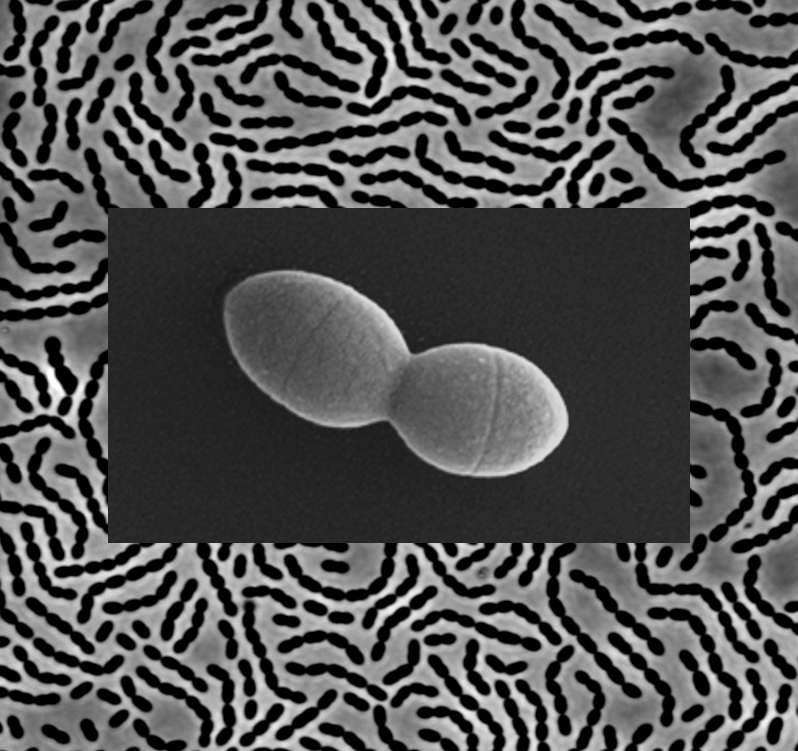 Streptococcus pneumoniae observée en microscopie à contraste de phase (arrière-plan) ; et zoom sur une seule cellule observée en microscopie électronique à balayage © Christophe Grangeasse
Streptococcus pneumoniae observée en microscopie à contraste de phase (arrière-plan) ; et zoom sur une seule cellule observée en microscopie électronique à balayage © Christophe Grangeasse
Streptococcus pneumoniae observée en microscopie à contraste de phase (arrière-plan) ; et zoom sur une seule cellule observée en microscopie électronique à balayage / © Christophe Grangeasse
Christophe Grangeasse et son équipe étudient également l’ensemble du cycle cellulaire du pneumocoque, pour dénicher une faille dans son système de résistance. Grâce à leur expertise sur les protéines de régulation PK et à une large panoplie de techniques, ils se penchent par exemple sur un mécanisme qui se déroule lors de l’assemblage de la paroi de Streptococcus pneumoniae. Christophe Grangeasse rappelle que « la synthèse du peptidoglycane (élément essentiel de la structure de cette paroi) fait intervenir de nombreuses protéines parmi lesquelles, les PBP (penicillin-binding proteins). Ces enzymes sont la cible privilégiée d’antibiotiques largement utilisés, comme la pénicilline ». Or, ces PBP sont sujets à des mutations génétiques qui permettent aux bactéries de développer une résistance à ces antibiotiques.
Pour prendre la bactérie à son propre jeu, les chercheurs ont choisi de se concentrer sur des protéines régulatrices des PBP. En changeant de cible, leur ambition est de concevoir des traitements qui permettraient de re-sensibiliser les souches résistantes aux antibiotiques, comme c’est le cas pour la pénicilline.
Déceler de nouveaux points faibles
Un étage au-dessus, Jean-Michel Jault et Cédric Orelle s’intéressent à une autre famille de protéines impliquées dans la résistance aux antibiotiques : les pompes à efflux. « Il s’agît de protéines membranaires capables de reconnaître plusieurs types d’antibiotiques et de les rejeter à l’extérieur des bactéries » expose Cédric Orelle. Leur objectif est donc de comprendre comment ces protéines fonctionnent, et quels sont les facteurs qui leur permettent de reconnaître tant d’antibiotiques différents. Pour ce faire, « nous adoptons une approche à la fois biochimique et structurale, déclare-t-il, qui se manifeste concrètement par le recours à des techniques de pointe, comme la cryomicroscopie électronique. »
Grâce à un travail collaboratif au sein d’un consortium de plusieurs équipes du laboratoire microbiologie moléculaire et biochimie structurale1, les chercheurs ont pu accéder à des images détaillées et inédites de la structure et révéler certains mouvements essentiels à l’activité de ces pompes à efflux. « Grâce à ces travaux, nous avons notamment pu obtenir de nouvelles informations sur le mécanisme de transport d’une pompe à efflux, poursuit Cédric Orelle, en mettant à jour ce qui favorise sa capacité à rejeter les antibiotiques et comment la protéine utilise l’énergie nécessaire à son fonctionnement ».
L’objectif est donc de comprendre les points forts et les points faibles de ces pompes à efflux, dans le but de faciliter la conception de traitements qui contournent leurs mécanismes de résistance. Les stratégies envisagées pourraient consister à les empêcher de capter de l’énergie, à bloquer leur mouvement pour qu’elles ne puissent plus expulser les médicaments hors de la bactérie, ou encore à contrarier leur capacité de reconnaissance des antibiotiques.
La bataille est encore longue, mais ces recherches prometteuses menées au laboratoire microbiologie moléculaire et biochimie structurale1 sont de nature à envisager sereinement l’avenir. Ces travaux très fondamentaux sont cruciaux pour décrire avec précision les mécanismes de régulation qui pourront être la clé de futurs traitements. Une perspective encourageante dans la lutte contre l’antibiorésistance.
Cet article fait partie d’un dossier thématique sur l’antibiorésistance "Résistances aux traitements : la recherche en quête de solutions" réalisé en collaboration avec Pop’Sciences - Université de Lyon (mai 2023).
--------------------
Ces recherches ont été financées en tout ou partie, par l’Agence Nationale de la Recherche (ANR) au titre des projets ANR-BIOTIFLUX et PEGASE -AAPG2019. Cette communication est réalisée et financée dans le cadre de l’appel à projet Sciences Avec et Pour la Société – Culture Scientifique Technique et Industrielle pour les projets JCJC et PRC des appels à projets génériques 2018-2019 (SAPS-CSTI-JCJ et PRC AAPG 18/19).




Commentaires
Connectez-vous, rejoignez la communauté
du journal CNRS